吉利德科学申报,ADC新药「戈沙妥珠单抗」在中国再获批临床!针对子宫内膜癌
转自:医药观澜
中国国家药监局药品审评中心(CDE)官网近日最新公示,由吉利德科学(Gilead Sciences)申报注射用戈沙妥珠单抗再次获批一项临床研究,适应症为用于既往接受过含铂化疗和抗程序性细胞死亡蛋白1/程序性细胞死亡配体1(抗PD-1/PD-L1)治疗后疾病进展的复发性或晚期子宫内膜癌患者。
截图来源:CDE官网
注射用戈沙妥珠单抗(sacituzumab govitecan,英文商品名:Trodelvy)是一款靶向Trop-2的抗体偶联药物(ADC)。TROP2在许多实体瘤中高表达,是ADC药物研发的热门靶点之一。戈沙妥珠单抗的设计是将拓扑异构酶抑制剂SN-38通过一款可水解的连接子与单克隆抗体连接在一起。这种组合能够将活性药物成分递送到表达Trop-2的细胞和微环境。
目前,戈沙妥珠单抗已在美国获批多项适应症,包括三阴性乳腺癌,HR+/HER2-乳腺癌和尿路上皮癌(mUC)等。与此同时,针对肺癌、头颈癌和子宫内膜癌的临床研究正在进行。
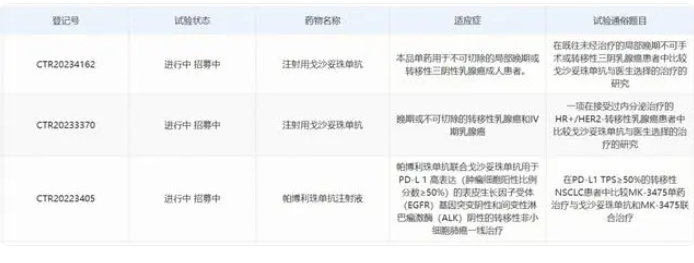
在中国,戈沙妥珠单抗最早于2022年获NMPA批准用于治疗局部晚期或转移性三阴性乳腺癌。根据中国药物临床试验登记与信息公示平台,戈沙妥珠单抗有三项临床研究正在开展。它们分别包括:
单药用于不可切除的局部晚期或转移性三阴性乳腺癌成人患者;
晚期或不可切除的转移性乳腺癌和IV期乳腺癌;
帕博利珠单抗联合戈沙妥珠单抗用于PD-L1高表达(肿瘤细胞阳性比例分数≥50%)的表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性的转移性非小细胞肺癌一线治疗。
子宫内膜癌是全球第二常见的妇科癌症,发病率和死亡率均在上升。虽然早期或局限性子宫内膜癌可以通过手术切除,患者预后良好,但晚期、转移/复发性子宫内膜癌患者的五年生存率不到20%。
此次注射用戈沙妥珠单抗再次获批临床,意味着这款ADC新药即将在中国开展针对子宫内膜癌的治疗。
本报道来源于网络,若有侵权请联系删除



 搜疾病
搜疾病 搜专家
搜专家 搜康复
搜康复


















